隨著全球人口高齡化加劇,如何延長「健康壽命」並精準干預「生物學年齡」已成為生物醫學的核心命題。近日,來自南方科技大學、電子科技大學、澳門科技大學、德國馬普進化生物學研究所、萊布尼茲老化研究所等國內外多家頂尖科研機構的跨學科專家團隊(我校朱健康校長為通訊作者之一),在國際衰老研究權威期刊 Ageing Research Reviews (IF=13, JCR Q1) 發表深度綜述。文章系統探討了利用線蟲、果蠅及非洲鱂魚等短壽命模型,結合自動化高通量篩選(HTS)與人工智能(AI)技術,在加速新型抗衰藥物(Geroprotectors)發現方面的最新突破、技術挑戰及臨床轉化路徑。

文章題目和參與作者
衰老是癌症、心血管疾病及神經退行性疾病共同的核心誘因。儘管現代醫學顯著延長了人類的平均壽命,但「健康壽命(Healthspan)」的增長卻並未同步,導致個體在晚年往往深陷失能與多病狀態。
在抗衰藥物研發管線中,傳統的細胞系模型難以模擬複雜的個體衰老,而斑馬魚、小鼠等脊椎動物模型雖具代表性,但其長達數年的壽命使得研發週期與成本極高。本綜述聚焦於與人類衰老機制高度保守的短壽命模型:線蟲與果蠅,並重點探討了非洲鱂魚這一脊椎動物「新星」在橋接轉化醫學中的關鍵作用,提出了一套整合多組學、自動化監控與 AI 視覺推理的「抗衰藥物發現新範式」。
一、 三大模型生物:抗衰藥物篩選的「先鋒隊」
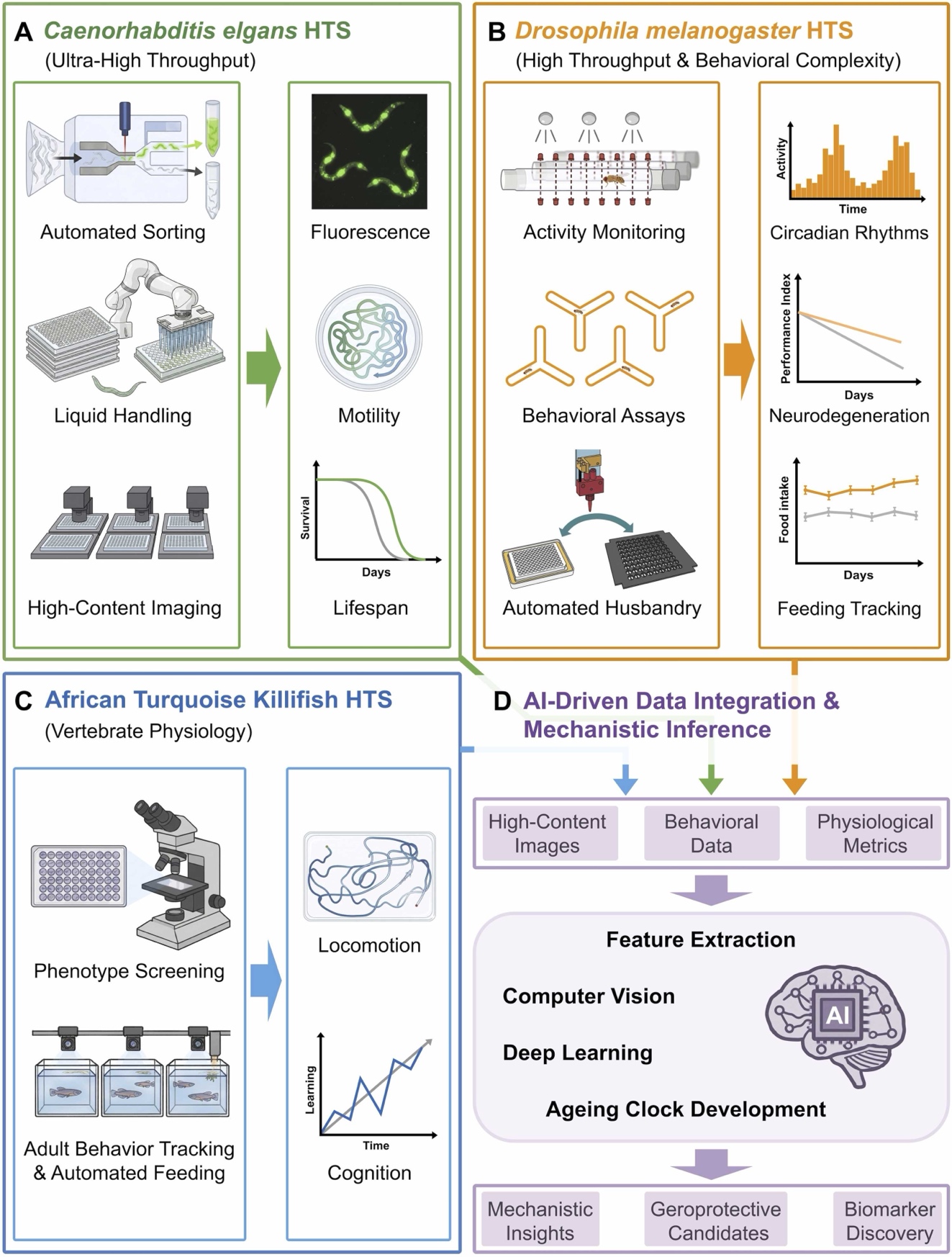
為了彌補體外實驗與人體臨床之間的巨大鴻溝,研究者正利用不同生物複雜度的模型構建梯度篩選平台(圖1):
秀麗隱桿線蟲(C. elegans): 憑藉 15-25 天的極短壽命及完全透明的身體,成為研究胰島素信號通路、線粒體應激及蛋白穩態失衡的經典首選模型。
黑腹果蠅(Drosophila): 擁有約 75% 的人類致病基因同源性。其 1-2 個月的壽命跨度,加之明確的性別差異與晝夜節律,使其成為研究中樞神經系統、腸道、肌肉衰老及性別特異性干預的理想平台。
非洲鱂魚(Killifish): 作為實驗室中最短命的脊椎動物(4-6 個月),它完美填補了無脊椎動物與哺乳動物之間的空白,具備脊椎動物特有的適應性免疫及複雜的組織再生能力。
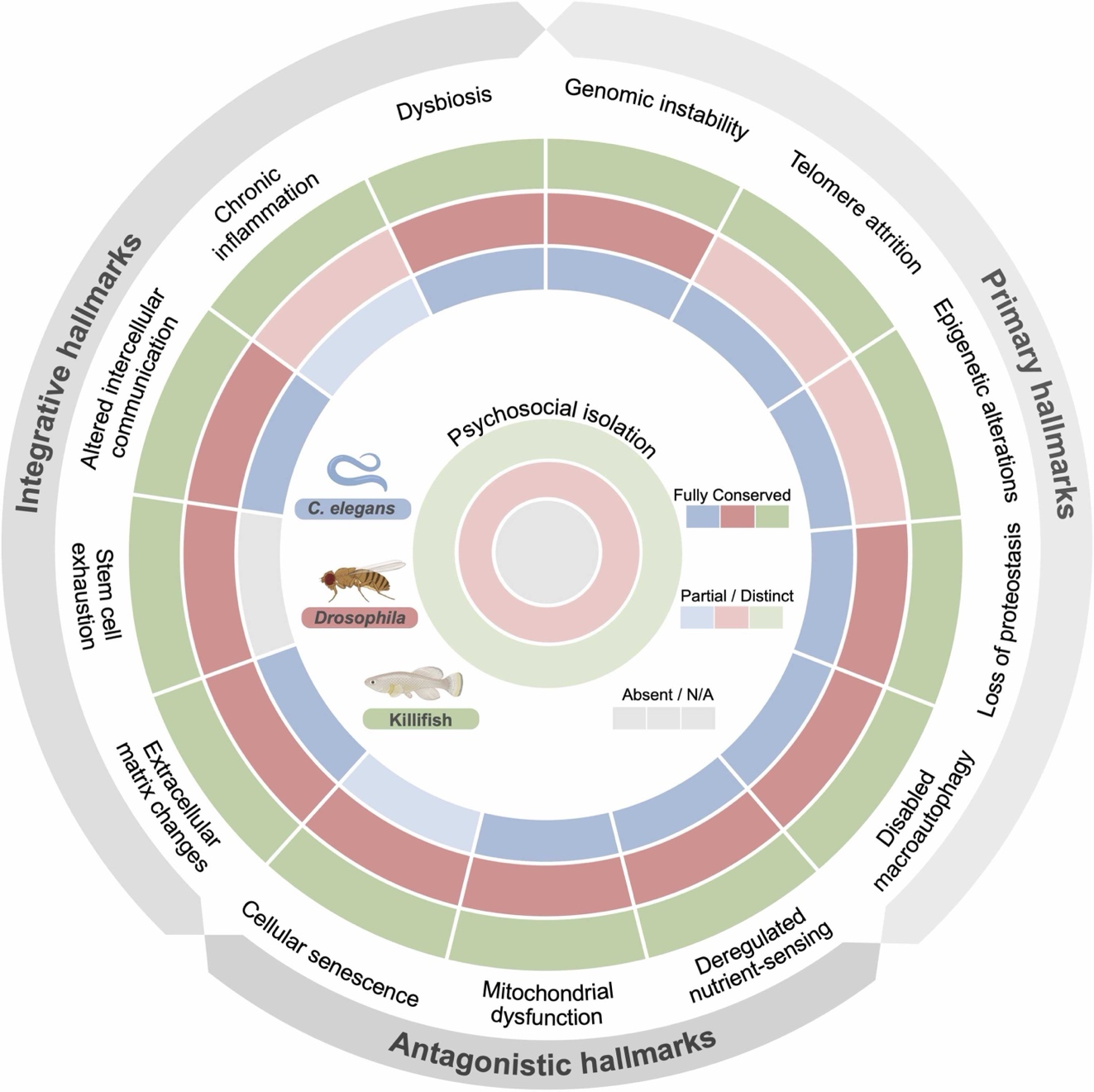
圖二:三種模型生物線蟲、果蠅以及非洲鱂魚,能夠重現絕大多數的衰老標誌物,為研究與人類衰老相關的保守通路以及發現抗衰藥物提供了極大的便利
二、 從「手動計數」到「數智化監測」
傳統的衰老研究高度依賴人工觀察,通量低且主觀性強。文章詳細介紹了 WormBot(線蟲機器人)、Lifespan Machine(壽命機器)及 DIAMonDS(果蠅個體活動監測系統) 等前沿硬體。
這些平台集成了高通量鏡頭追蹤、微流控晶片和紅外感測技術,實現了對成千上萬個實驗個體從出生到死亡的全生命週期自動化監控。這種「無人值守」的檢測模式不僅極大提升了篩選通量,更確保了數據的客觀性與可重複性。
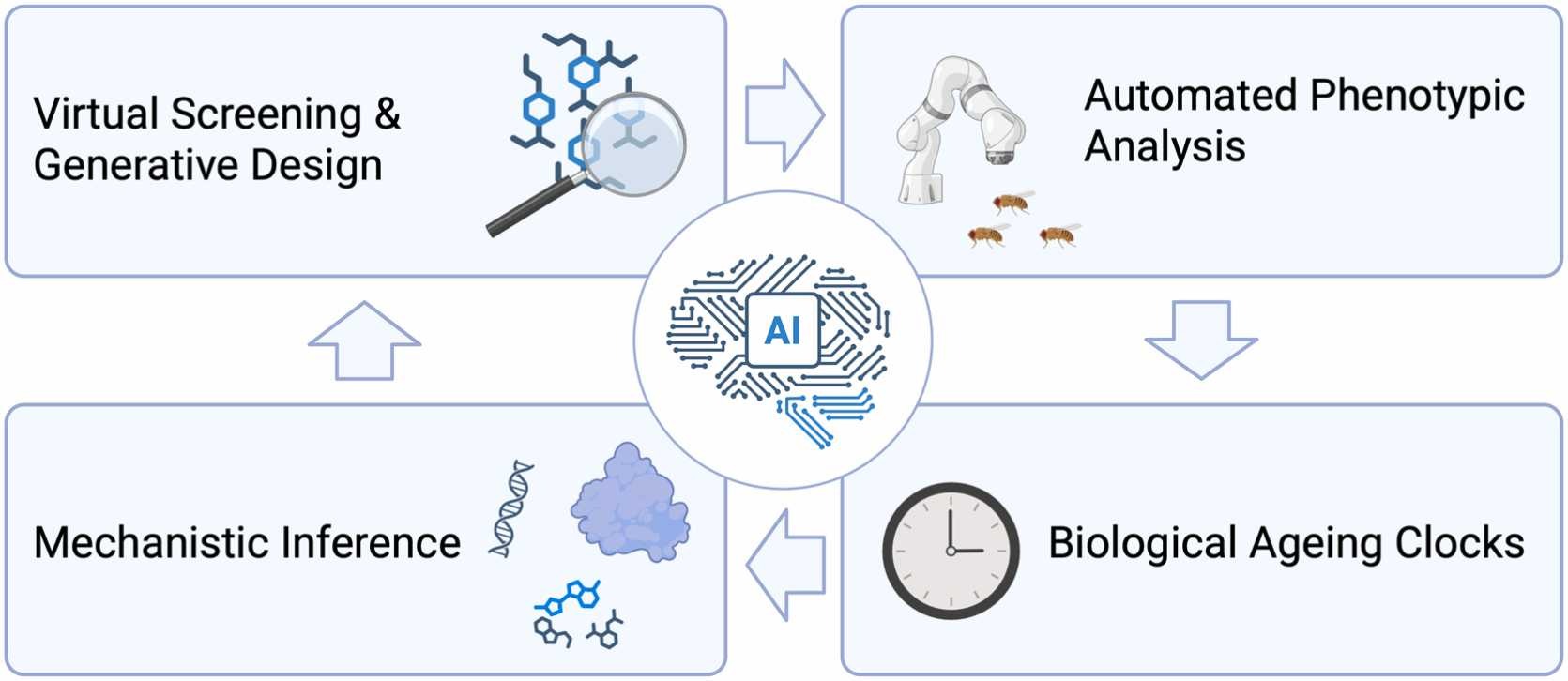
圖3:透過以下技術強化了衰老研究與藥物開發中高通量篩選(HTS)的各個階段:虛擬與生成式化合物設計,自動化表型篩選,生物學衰老時鐘,機制分析
三、 靶向衰老標識:從「活得久」到「老得慢」
綜述強調,現代篩選目標已從單純的「延長壽命」轉向對衰老標誌物(Hallmarks of Ageing)的深度干預:
原發性標誌物: 利用螢光報告系統實時監測體內蛋白穩態(Proteostasis)失衡與氧化應激水平。
拮抗性標誌物: 動態追蹤線粒體形態演變(從網絡狀到碎片化),篩選精準改善線粒體功能的代謝調節劑。
綜合性標誌物:
“藍精靈(Smurf)”實驗: 通過監測腸道完整性受損導致的“全身藍色滲漏”表型,提前預判個體死亡風險,成為評估腸道屏障與系統性炎症的關鍵指標。
行為組學追蹤: 史丹福大學等團隊開發的聯網自動化餵食系統,不僅能精確控制熱量攝取,還能開展複雜的視覺關聯學習實驗,從而評價藥物對脊椎動物認知功能及社交行為的改善作用。
四、 “反向翻譯”策略:加速老藥新用
不同於傳統的「從實驗室到臨床」的線性邏輯,綜述特別強調了「反向翻譯(Reverse Translation)」的巨大潛力。以二甲雙胍(Metformin)、SGLT2 抑制劑及 GLP-1 受體激動劑為例,這些藥物最初用於代謝性疾病,但在人群大規模流行病學數據中展現了顯著的抗衰老潛力。通過在短壽命模型中進行快速、高通量的機制驗證,研究者得以迅速釐清其是否通過保守的長壽通路(如 AMPK 或 mTOR)發揮作用,極大地縮短了藥物從「臨床發現」到「機制確認」再到「廣泛應用」的週期。
未來的衰老藥物發現將是「乾濕結合」的混合管線:從 AI 輔助的億級分子虛擬設計,到自動化機器人平台的生物驗證,再到器官晶片(Organ-on-a-chip)的人體模擬。這一閉環系統正以前所未有的速度縮短研發週期,助力人類跨越「健康鴻溝」,向「健康老齡化」的目標全速前進。
本文第一作者為南方科技大學醫學院/前沿生物技術研究院吉興坤博士生、雷家俊碩士生,以及電子科技大學醫學院潘彥本科生。通訊作者包括南方科技大學呂宇軒教授、電子科技大學鮮波教授、澳門科技大學朱健康院士、德國萊布尼茲老化研究所/意大利比薩大學 Alessandro Cellerino 教授、德國馬普進化生物學所/基爾大學 Judith Bossen 博士等。此外,研究得到了南方科技大學工學院陳放怡教授、中科院上海營養與健康研究所陸炯明研究員以及多個海內外研究機構的支持。





